Десублимация — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 мая 2015; проверки требуют 13 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 мая 2015; проверки требуют 13 правок.
Десублима́ция (Депози́ция) — физический процесс перехода вещества из газообразного состояния в твёрдое, минуя жидкое. При десублимации высвобождается энергия. Десублимация является экзотермическим фазовым переходом. Обратным процессом является возгонка (сублимация). Десублимация осуществляется на твёрдые поверхности или происходит в объёме газовой фазы с выделением твердого вещества в виде частиц аэрозоля.
При десублимации (процесс самоорганизации) возникают ван-дер-ваальсовы связи между отдельными молекулами вещества с выделением энергии, которую отводят от десублимата непосредственным контактом его с охлаждаемой твёрдой поверхностью, взаимодействуя с вводимым дополнительно хладагентом, испарением жидкости, добавляемой в газовую смесь, её расширением.
Примером десублимации является появление ледяных узоров на оконных стёклах в зимнее время и такие атмосферные явления, как иней и изморозь.
Десублимационные процессы используются во всех отраслях народного хозяйства: химической, пищевой, металлургической, электронной и других. Эти процессы применяют для выделения веществ из парогазовых смесей на охлаждаемых поверхностях и в объеме, для получения новых твердых продуктов в результате химической реакции между исходными газообразными реагентами, для очистки веществ, для образования твердых покрытий, сублимационной сушки термочувствительных материалов.
Что такое сублимация в физике? Примеры
Наверняка, каждый человек не раз сталкивался с понятием сублимации в физике. В школах этой теме всегда посвящают несколько уроков, а в высших учебных заведениях, направленных на более глубокое изучение точных наук, ей уделяют особое внимание. Итак, в статье вы узнаете, что такое сублимация и десублимация в физике.
Общее понятие
Сублимация в физике — это процесс перехода вещества из твердого состояние в газообразное, минуя при этом жидкое. По-другому она называется взгонкой вещества. Этому процессу сопутствует поглощение энергии (в физике эта энергия имеет название «теплота сублимации»). Процесс является очень важным и имеет широкое применение в экспериментальной физике.
Десублимация — это, напротив, процесс перехода вещества из газообразного в твердое состояние. Еще одно название данного процесса — «депозиция». Она является полностью противоположной сублимации. При депозиции энергия выделяется, а не поглощается, причем в очень больших количествах. Десублимация также является очень важной, однако намного сложнее привести пример ее целенаправленного использования человеком, особенно в быту.
Описание процесса
Катализаторами сублимации в физике может служить почти все, что угодно. Иногда вещества сублимируются (так называется этот самый процесс в физике), когда достигают определенной температуры. Как правило, речь идет о температуре выше средней, однако есть некоторые исключения, когда вещества «взгоняются» при отрицательных значениях.
Иногда катализатором этого процесса может являться кислород. В таких случаях вещество будет переходить в газообразное вещество при контакте с воздухом. Кстати говоря, такой прием зачастую используется режиссерами в фантастических фильмах. Здорово, не правда ли?!
Для десублимации катализаторы ровным счетом аналогичные, однако нужно уловить одну закономерность: все параметры, за исключением некоторых особых химических реакций, будут с отрицательным знаком. То есть, если при сублимации основная масса процессов происходит при положительных температурах, то при депозиции, напротив, будут фигурировать низкие.
Стоит также отметить, что переход происходит последовательно. Каждому промежутку времени соответствует свой его перехода.

Многие ученые даже разделяют его на стадии, но этого можно и не делать. Применим это он к взгонке, так и к обратному ей процессу. Именно это позволяет физикам контролировать процесс и использовать его даже в быту.
Примеры
Существует множество примеров сублимации в физике, однако и примеров обратного ей процесса тоже довольно много. Стоит рассмотреть обе категории.
Итак, примеры взгонки:
- Сухой лед.
 Наверное, это самый распространенный пример процесса. Наверняка, каждый хоть раз видел или держал в его руках. Одно время сухой лед был крайне популярным предметом для съемок видео на «Ютубе». Почти каждый человек видел хотя бы одно такое видео. Стоит отметить, что лед используется не только в развлекательных целях. Он также имеет довольно широкое применение в быту.
Наверное, это самый распространенный пример процесса. Наверняка, каждый хоть раз видел или держал в его руках. Одно время сухой лед был крайне популярным предметом для съемок видео на «Ютубе». Почти каждый человек видел хотя бы одно такое видео. Стоит отметить, что лед используется не только в развлекательных целях. Он также имеет довольно широкое применение в быту. - Высыхание белья на морозе.
 Абсолютно каждая хозяйка зимой вывешивает белье на мороз. Казалось бы, оно должно вернуться застывшим, однако возвращается полностью сухим. Связано это с тем, что произошла сублимация молекул воды. Это самый наглядный пример применения сублимации в физике.
Абсолютно каждая хозяйка зимой вывешивает белье на мороз. Казалось бы, оно должно вернуться застывшим, однако возвращается полностью сухим. Связано это с тем, что произошла сублимация молекул воды. Это самый наглядный пример применения сублимации в физике.
Самое время перейти к депозиции. Целесообразно рассмотреть примеры:
- Иней.
 Это самый наглядный пример десублимации в природе, с которым связывался абсолютно каждый. Происходит процесс при крайне резком похолодании и слишком быстром прохождении точки росы. Такое явление широко распространено. Увидеть иней можно поздней осенью и зимой. Наиболее хорошо различим он в октябре-ноябре, когда снега еще совсем немного.
Это самый наглядный пример десублимации в природе, с которым связывался абсолютно каждый. Происходит процесс при крайне резком похолодании и слишком быстром прохождении точки росы. Такое явление широко распространено. Увидеть иней можно поздней осенью и зимой. Наиболее хорошо различим он в октябре-ноябре, когда снега еще совсем немного. - Узор на окнах зимой.
 Да, оказывается именно десублимация создает нашу новогоднюю атмосферу. Замысловатые узоры возникают из-за огромнейшей разницы между температурами на улице и в помещении.
Да, оказывается именно десублимация создает нашу новогоднюю атмосферу. Замысловатые узоры возникают из-за огромнейшей разницы между температурами на улице и в помещении.
Для чего она нужна
Процесс сублимации, помимо того, что он часто встречается в природе, нашел широкое распространение в бытовых вопросах. Обусловлено это удобством, а также малой токсичностью вещей, склонных к этому процессу. Итак, вот несколько примеров ее использования в быту:
- Сушка белья. Как было сказано выше, молекулы воды просто выветриваются, минуя одно из агрегатных состояний. Такой способ сушки до сих пор остается чуть ли не самым популярным.
- Принтеры цветной печати. Твердые цветные частицы краски сразу переходят в газообразное состояние под воздействием давления и температуры. Несмотря на то, что такой способ уходит в прошлое, кое-где он распространен и в наше время.
- Средства от моли и ароматические пластинки. Нередко какой-то из этих предметов можно найти в шкафу. Такие пластинки не просто растворяются, как многие думают, а переходят в состояние газа и переносят запах.
Помимо этого, сублимация широко используется в разнообразных физических опытах. Интересно отметить, что в химии способность веществ к сублимации нередко является основополагающей причиной качественной реакции.
Где еще встречается этот термин
Термин «сублимация» можно встретить не только в физике и химии. Также он уместен и в психологии. В этой науке его расшифровка совсем иная: это способ «выпустить пар», кардинально изменив свой вид деятельности.
Также термин используется в стези печати. В этой сфере деятельности определение меняется: сублимационная печать — это один из способов переноса изображения на любую поверхность с помощью краски, которая проходит процесс взгонки. Проще говоря, это один из способов печати на любой поверхности.
Заключение
В заключении данной статьи следует заметить, что сублимация, даже несмотря на то, что ее понятие встречается в самых разных сферах деятельности общества, в первую очередь остается физическим термином. Именно оттуда, как говорится, «растут ноги». Внимательно вчитайтесь в определение сублимации в физике, а потом сравните его со всеми остальными расшифровками. Таким образом, вы увидите, что термины схожи по своему значению. Дело в том, что каждый из них адаптирован под ту или иную сферу деятельности, о которой идет речь.
Лекция «Сублимация и десублимация. Плавление и кристализация»
Лекция № 15
Плавление и кристаллизация. Понятие о фазе вещества. Сублимация и десублимация.
Кристаллизация – это переход вещества в кристаллическое состояние из жидкого, или газообразного, или аморфного состояния.
Кристаллизация является фазовым переходом, происходит с выделением тепла, но при постоянной температуре. Примеры кристаллизации: замерзание воды (переход из жидкой фазы в кристаллическую), образование инея (переход из газообразной фазы в кристаллическую).
Плавление кристаллического вещества – это переход из кристаллической фазы в жидкую.
Процесс плавления кристаллического вещества происходит с поглощением тепла, но температура остается постоянной, пока плавление не завершится. Пример плавления кристаллического вещества – таяние льда. Смесь снега и льда сохраняет температуру 0° С, пока весь лед не растает.
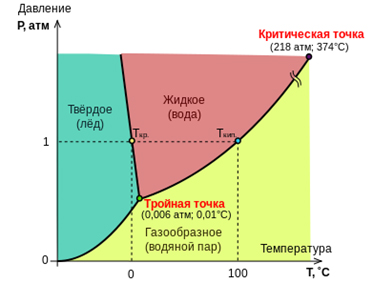
Фазовые переходы на диаграмме температуры и давления
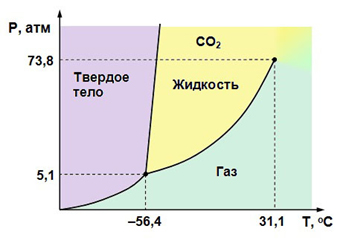
Лед, вода, пар – классический пример трех агрегатных состояний вещества. Не всегда вещества демонстрируют такие же «правильные» фазовые переходы. Например, углекислый газ замерзает и переходит в кристаллическую фазу при температуре -56,6°С, минуя жидкую фазу. При нагревании твердый диоксид углерода не плавится, а испаряется, переходя сразу в газообразное состояние. Но при более высоких температурах и высоком давлении возможен переход диоксида углерода в жидкое состояние, а при дальнейшем охлаждении жидкой фазы происходит кристаллизация.
Кристаллизация и затвердевание: в чем разница?
Твердые вещества могут не быть кристаллическими. Например, стекло и стеклоподобные аморфные вещества постепенно затвердевают при остывании; у них нет явно выраженной точки фазового перехода. Плавление стекла тоже происходит в некотором диапазоне температур, зависящем от химического состава и наличия примесей.
если тепло не подводить, то жидкая и твердая фазы будут оставаться в равновесии;
если тепло поступает, то кристаллы будут плавиться, при сохранении температуры фазового перехода;
если тепло отводить, то происходит рост кристаллов, температура фазового перехода сохраняется, пока вся жидкая фаза не перейдет в кристаллическую.
Например, смесь воды со льдом в жаркий день сохраняет нулевую температуру, пока весь лед не растает. Поступающее тепло увеличивает внутреннюю энергию за счет приобретения молекулами дополнительных степеней свободы, но температура сохраняется прежняя до того, как лед полностью растает.
Фазовый переход в твердом веществе между двумя кристаллическими состояниями
Иначе ведет себя углерод. У него несколько фазовых переходов. Из жидкой формы, при отводе тепла, он переходит в кристаллическую фазу – графит; при высоком давлении более 120 000 атм. жидкий углерод кристаллизуется в алмаз.
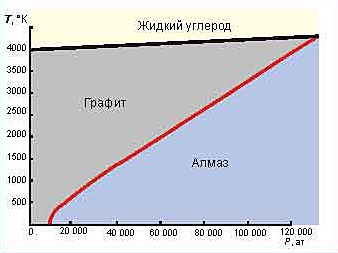
На рисунке красной линией показана диаграмма фазового перехода между алмазом и графитом. Температура фазового перехода зависит от давления, процессы, происходящие в твердом теле, аналогичны кристаллизации воды: если тепло подводить, то алмаз переходит в графит; если тепло отводить при соответствующем высоком давлении, то происходит переход, кристаллизация графита в алмаз.
Кристаллизация жидких кристаллов
Есть вещества, имеющие несколько кристаллических фаз в твердом состоянии; но есть целый класс веществ, имеющих несколько фазовых переходов в жидком состоянии: это вещества, раствор или расплав которых образует жидкие кристаллы.
Жидкие кристаллы – это частично упорядоченные двумерные или одномерные структуры. Они стабильны в узком диапазоне температур, являются промежуточным состоянием между кристаллической и жидкой фазами. Переход от трехмерной кристаллической решетки к двумерной или одномерной структуре происходит при температуре фазового перехода; после того, как весь образец перейдет в жидкокристаллическое состояние, температура начинает повышаться, и повышается до значения, соответствующего следующему фазовому переходу. В конце концов частично упорядоченная структура переходит в жидкую фазу, при температуре соответствующего фазового перехода.
Сублимация и десублимация.
Процесс перехода твёрдых тел в газообразное состояние, минуя жидкую стадию, называют сублимацией, или возгонкой.
Испарение происходит и в твёрдых телах. Мы видим, как постепенно высыхает на морозе замёрзшее, покрытое льдом бельё. Мы ощущаем запах, образующийся при испарении твёрдого вещества мыла. То есть твердое тело превращается в пар.
Сублимация
ТВ. ТЕЛО  ПАР
ПАР
Десублимация
Иногда вещество может перейти из газообразного состояния сразу в твёрдое, минуя жидкую стадию. Такой процесс называется десублимацией.
Десублимация — это переход из газообразного состояния сразу в твердое.
Ледяные узоры, которые появляются на стёклах в мороз, и есть пример десублимации. При заморозках почва покрывается инеем — тонкими кристалликами льда, в которые превратились водяные пары из воздуха.
Десублимация
ПАР  ТВ.ТЕЛО
ТВ.ТЕЛО
СУБЛИМАЦИЯ И ДЕСУБЛИМАЦИЯ • Большая российская энциклопедия
-

-

-

В книжной версии
Том 31. Москва, 2016, стр. 361
-

Скопировать библиографическую ссылку:
Авторы: Э. Г. Раков
СУБЛИМА́ЦИЯ И ДЕСУБЛИМА́ЦИЯ, переход вещества из твёрдого состояния в газообразное и обратно без образования расплава при изменении темп-ры. Термин «сублимация» (от лат. sublimo – возносить) эквивалентен возгонке. С. и д. относятся к фазовым переходам 1-го рода и сопровождаются тепловыми эффектами: поглощением теплоты при сублимации и выделением при десублимации. Оба процесса протекают при темп-рах и давлениях ниже тех, что соответствуют тройной точке рассматриваемого вещества. Десублимация может осуществляться на холодной поверхности или при смешении паров вещества с более холодным газом, при расширении некоторых сжатых газов (образование твёрдого диоксида углерода при работе огнетушителей).
Процессы С. и д. происходят в естеств. условиях, применяются в лабораторной практике и в пром-сти. Напр., образование снега, инея, морозных узоров на оконных стёклах является десублимацией атмосферной влаги при охлаждении её паров ниже 0 °С, испарение намёрзшего льда и выпавшего снега при темп-рах ниже 0 °С – сублимацией. В пром-сти С. и д. используют для выделения веществ из газовых потоков (напр., фталевого ангидрида, гексафторида урана), очистки веществ, сублимац. сушки (напр., пищевых продуктов), тепловой защиты ЛА при сверхзвуковых скоростях полёта, нанесения защитных и функциональных покрытий при изготовлении приборов и др.
что это простыми словами в различных областях химии, психологии, промышленности

Понятие «сублимация» имеет разные значения. Смысл этого выражения зависит от области, в которой оно применяется. Вы могли узнать о сублимации из трудов психологов, заметить это слово в статьях про пищевую промышленность или услышать в школе.
Специфика каждого определения уникальна. Мы разберём понятия сублимации вместе со сферами их применения, подкрепим всё это житейским опытом и разложим полученные знания по полочкам.
Значение слова сублимация
С научной позиции, сублимация – это когда вещество переходит из твёрдого состояния в состояние газа, и при этом упускает стадию жидкости.

Психологическая сублимация – это защитная реакция психики, которая возникает из-за внутреннего напряжения. Она перенаправляет неизрасходованную энергию на положительные поступки или творчество.
В химии
Впервые о сублимации и десублимации мы узнаём ещё в школе на уроке химии, где нам рассказывают, что она идёт под руку с тепловыми явлениями и фазами вещества. Позже с ней сталкиваются студенты технических колледжей и университетов. Но изучают они эту тему куда глубже, чем нас сейчас интересует.
Читайте также: Что значит Кворум, МРОТ, Толерантность и Диверсификация
Ещё такой процесс принято называть взгонкой вещества. Во время сублимации вещество поглощает энергию, то есть определённое количество теплоты, которое носит название «теплота сублимации». Если вещество не поглотит нужную ему теплоту, то процесс не случится.

Десублимация работает по такому же принципу, только наоборот. Цель депозиции (другое название десублимации) – переход газообразного вещества в твёрдое. Энергия в процессе не поглощается, а наоборот, выделяется.
Ускорить реакцию сублимации может подходящий температурный режим, который устанавливается в зависимости от используемого вещества. И не всегда в таком случае имеется в виду именно высокая температура.
При низких значениях взгонка тоже возможна, а вот десублимация в большинстве случаев будет проходить только при отрицательных температурах.
Ещё в качестве катализатора (ускорителя) может быть применён кислород, и тогда вещество перейдёт в состояние газа из-за своего контакта с воздухом.
Чтобы осознать масштаб работы этих процессов достаточно зимой вывесить на открытый балкон мокрую одежду. Спустя пару часов она вернётся в дом сухая и вымороженная.

Дело в том, что на улице с вашим бельём происходило множество маленьких приключений.
- Сначала вода кристаллизовалась в лёд, то есть произошёл переход из жидкой стадии в твёрдую – это отправная точка сублимации.
- Затем крошки-кристаллы испарились под прямыми лучами солнца. Это значит, что твёрдые тела поглотили нужное им для испарения количество теплоты и перешли в газообразное состояние.
Десублимация действует иначе: она создаёт лёд. К примеру, вы просыпаетесь, выходите из дома и видите вокруг результат депозиции – иней. Он образовался из водяного пара, который всегда ненавязчиво преследует нас в окружающей среде.
Морозным утром, когда температура земли упала до отрицательного значения, водяной пар соприкоснулся с травой. Тогда-то и пошёл процесс десублимации, и в итоге трава покрылась корочкой льда.

Теперь, после знакомства с базовыми понятиями, мы перейдём к теме применения сублимации на производстве.
В промышленности
Круг применения сублимации включает в себя самые разные сферы производства: пищевую и химическую промышленность, полиграфию, лабораторные исследования.
Остановимся подробнее на теме полиграфии.
Сублимационная печать – это цифровой метод печати, при котором изображение с бумаги под прессом переносится на запечатываемый материал: синтетическую ткань, алюминий, керамику и стеклопластик.
В производстве используется термопресс – устройство, в котором под давлением и температурой, достигающей 200оС, происходит перенос изображение на предмет.
Это возможно благодаря специальным, сублимационным чернилам. Они содержат красители, частицы которых способны испаряться под воздействием высокой температуры.

В качестве запечатываемого материала выступают светлые синтетические ткани, потому что они имеют более рыхлую структуру, по сравнению с натуральными. Такая структура даёт чернилам возможность активно впитываться в материю, а светлый цвет ткани позволяет добиться насыщенной картинки.
Процесс переноса изображения на футболку выглядит таким образом:
- На компьютере подготавливается изображение, затем оно выводится на печать через струйный принтер.
- Для печати подбирается бумага, способная без затруднений отдавать краситель со своей поверхности другому материалу.
- Затем изображение приклеивают к футболке скотчем, выдерживающим температуру термопресса, и помещают под разогретый пресс. Чернила испаряются в ткань и окрашивают её.
С помощью сублимации запечатывают сувенирную продукцию разных объёмов: от единичных экземпляров до сотенных тиражей.
А вот пищевая промышленность использует сублимацию для сушки продуктов. Сначала еда резко охлаждается до образования кристалликов льда, затем сублимируется, ужимается в вакууме. Сам процесс называется лиофилизация.

При увлажнении сублимированного продукта, происходит возвращение в исходное состояние. Это легко проследить на примере растворимого кофе. Сначала он представляет собой кофейный концентрат, потом сублимированный кофе, а после контакта с водой – напиток.
С понятием из области науки и промышленности мы разобрались. Впереди нас ждёт гуманитарное знание.
В психологии
Это понятие было введено в психологическую науку Зигмундом Фрейдом, знаменитым австрийским психоаналитиком.
Фрейд описывал сублимацию со стороны сексуального влечения, которое направляется от своей цели к достижению целей, приемлемых социумом.

По большему счёту, сублимация — это переход накопившейся энергии в действия.
Как эффективно сублимировать и почему это полезно
Сублимировать полезно, потому что это разгружает психику, даёт возможность человеку шире взглянуть на ситуацию и найти безопасную и положительную форму активности для выплёскивания своих чувств.
Небольшая инструкция:
- Расслабьтесь. Жизнь вокруг не останавливается, пока вы сосредоточены на своём состоянии.
- Пробуйте мечтать. Перебирайте все варианты, которые только приходят в голову. Однажды вы за что-нибудь зацепитесь и поймёте – это то, к чему вам хочется стремиться.
- Медитируйте. Глубокая медитация, при правильном своём проведении, поможет докопаться до внутреннего «я» и узнать чем это «я» хочет заниматься и какое решение проблем предпочтёт.
- Влюбляйтесь. И запоминайте своё состояние. С таким же чувством эйфории нужно приступать к выполнению выбранной цели.
Примеры из жизни
Саша чувствует обиду на коллег, которые свалили на него всю работу в пятницу вечером и уехали по домам. Вместо проявления агрессии, на следующий день он идёт на стадион и пробегает 10 километров.

Лиза любит Лёшу, но вместо того чтобы заигрывать с ним, она вдохновлённо пишет по вечерам картины, тяжко вздыхая по возлюбленному.

Лёша тоже любит Лизу и поэтому сутками играет в онлайн-игры, направляя свою неизрасходованную сексуальную энергию на азарт завоевания очередного королевства.

Теперь вы знаете, что помогает мокрым полотенцам высыхать зимой, как связаны лиофилизация с растворимым кофе и почему влюблённые носят с собой тетрадку со стихами. Это всё многогранная сублимация.
Сублимация (физика) — это… Что такое Сублимация (физика)?
У этого термина существуют и другие значения, см. Сублимация.  | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 15 мая 2011. |
Сублимация (возго́нка) — переход вещества из твёрдого состояния сразу в газообразное, минуя жидкое. Поскольку при возгонке изменяется удельный объём вещества и поглощается энергия (теплота сублимации), возгонка является фазовым переходом первого рода.
Обратным процессом является десублимация. Примером десублимации являются такие атмосферные явления, как иней на поверхности земли и изморозь на ветвях деревьев и проводах.
Примеры возгонки
Сублимация иода
Возгонка характерна, например, для элементарного иода I2, который при нормальных условиях не имеет жидкой фазы: чёрные с голубым отливом кристаллы сразу превращаются (сублимируются) в газообразный молекулярный иод (медицинский «йод» представляет собой спиртовой раствор).
Сублимация льда
Хорошо поддается возгонке лёд, что определило широкое применение данного процесса как одного из способов сушки. При промышленной возгонке сначала производят заморозку исходного тела, а затем помещают его в вакуумную или заполненную инертными газами камеру. Физически процесс возгонки продолжается до тех пор, пока концентрация водяных паров в камере не достигнет нормального для данной температуры уровня, в связи с чем избыточные водяные пары постоянно откачивают. Возгонка применяется в химической промышленности, в частности, на производствах взрывоопасных или взрывчатых веществ, получаемых осаждением из водных растворов.
Применение процесса
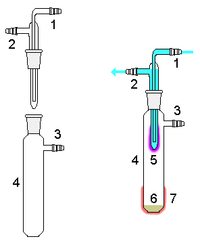 Простой сублимационный аппарат. Очищаемое вещество конденсируется из газовой фазы на «пальце»-холодильнике, охлаждаемом водой.
Простой сублимационный аппарат. Очищаемое вещество конденсируется из газовой фазы на «пальце»-холодильнике, охлаждаемом водой.1 Вход холодной воды
2 Выход холодной воды
3 Вакуум/газ линия
4 Сублимационная камера
5 Сублимируемый продукт
6 Сырой материал
7 Внешний нагрев
Применение сублимации в лабораторной технике
На эффекте возгонки основан один из способов очистки твердых веществ. При определенной температуре одно из веществ в смеси возгоняется с более высокой скоростью, чем другое. Пары очищаемого вещества конденсируют на охлаждаемой поверхности. Прибор, применяемый для этого способа очистки, называется сублиматор.
Сублимационная сушка
Основная статья: Сублимационная сушка
Сублимационная сушка (иначе лиофилизация; лиофильная сушка) (англ. freeze drying или lyophilization) — процесс удаления растворителя из замороженных растворов, гелей, суспензий и биологических объектов, основанный на сублимации затвердевшего растворителя (льда) без образования макроколичеств жидкой фазы[1].
Возгонка также используется в пищевой промышленности: так, например, сублимированный кофе получают из замороженного кофейного экстракта через обезвоживание вакуумом. Фрукты после сублимирования весят в несколько раз меньше, а восстанавливаются в воде. Сублимированные продукты значительно превосходят сушеные по пищевой ценности, так как возгонке поддаётся только вода, а при термическом испарении теряются многие полезные вещества. Перед сублимацией пищевых продуктов используется быстрое замораживание (от −100 до −190 °C), что приводит к образованию мелких кристаллов, не разрушающих клеточные мембраны.
См. также
Примечания
Ссылки
Сублимация (физика) | Virtual Laboratory Wiki
Файл:Sublimation apparatus.pngВозго́нка (сублимация) — переход вещества из твёрдого состояния сразу в газообразное, минуя жидкое. Поскольку при возгонке изменяется удельный объём вещества и поглощается энергия (теплота сублимации), возгонка является фазовым переходом первого рода. Обратным процессом является десублимация.
Примеры возгонки
Сублимация йода
Возгонка характерна, например, для элементарного йода I3, который при нормальных условиях не имеет жидкой фазы: чёрные с голубым отливом кристаллы сразу превращаются (сублимируются) в газообразный молекулярный йод (медицинский «йод» представляет собой спиртовой раствор).
Известным примером десублимации является появление инея на ветках во время усиления мороза.
Сублимация воды
Хорошо поддается возгонке вода, что определило широкое применение данного процесса как одного из способов сушки. При промышленной возгонке сначала производят заморозку исходного тела, а затем помещают его в вакуумную или заполненную инертными газами камеру. Физически процесс возгонки продолжается до тех пор, пока концентрация водяных паров в камере не достигнет нормального для данной температуры уровня, в связи с чем избыточные водяные пары постоянно откачивают. Возгонка применяется в химической промышленности, в частности, на производствах взрывоопасных или взрывчатых веществ, получаемых осаждением из водных растворов.
Применение процесса
Применение сублимации в лабораторной технике
На эффекте возгонки основан один из способов очистки твердых веществ. При определенной температуре одно из веществ в смеси возгоняется с более высокой скоростью чем другое. Пары очищаемого вещества конденсируют на охлаждаемой поверхности. Прибор, применяемый для этого способа очистки, называется сублиматор.
Сублимационная сушка
Возгонка также используется в пищевой промышленности: так, например, фрукты после сублимирования весят в несколько раз меньше, а восстанавливаются в воде. Сублимированные продукты значительно превосходят сушеные по пищевой ценности, так как возгонке поддаётся только вода, а при термическом испарении теряются многие полезные вещества. Перед сублимацией пищевых продуктов используется быстрое замораживание (-100 до -190 град. Цельсия), что приводит к образованию мелких кристаллов, неразрушающих клеточные мембраны.
См. также
Ссылки
Эта страница использует содержимое раздела Википедии на русском языке. Оригинальная статья находится по адресу: Сублимация (физика). Список первоначальных авторов статьи можно посмотреть в истории правок. Эта статья так же, как и статья, размещённая в Википедии, доступна на условиях CC-BY-SA .
 Наверное, это самый распространенный пример процесса. Наверняка, каждый хоть раз видел или держал в его руках. Одно время сухой лед был крайне популярным предметом для съемок видео на «Ютубе». Почти каждый человек видел хотя бы одно такое видео. Стоит отметить, что лед используется не только в развлекательных целях. Он также имеет довольно широкое применение в быту.
Наверное, это самый распространенный пример процесса. Наверняка, каждый хоть раз видел или держал в его руках. Одно время сухой лед был крайне популярным предметом для съемок видео на «Ютубе». Почти каждый человек видел хотя бы одно такое видео. Стоит отметить, что лед используется не только в развлекательных целях. Он также имеет довольно широкое применение в быту. Абсолютно каждая хозяйка зимой вывешивает белье на мороз. Казалось бы, оно должно вернуться застывшим, однако возвращается полностью сухим. Связано это с тем, что произошла сублимация молекул воды. Это самый наглядный пример применения сублимации в физике.
Абсолютно каждая хозяйка зимой вывешивает белье на мороз. Казалось бы, оно должно вернуться застывшим, однако возвращается полностью сухим. Связано это с тем, что произошла сублимация молекул воды. Это самый наглядный пример применения сублимации в физике. Это самый наглядный пример десублимации в природе, с которым связывался абсолютно каждый. Происходит процесс при крайне резком похолодании и слишком быстром прохождении точки росы. Такое явление широко распространено. Увидеть иней можно поздней осенью и зимой. Наиболее хорошо различим он в октябре-ноябре, когда снега еще совсем немного.
Это самый наглядный пример десублимации в природе, с которым связывался абсолютно каждый. Происходит процесс при крайне резком похолодании и слишком быстром прохождении точки росы. Такое явление широко распространено. Увидеть иней можно поздней осенью и зимой. Наиболее хорошо различим он в октябре-ноябре, когда снега еще совсем немного. Да, оказывается именно десублимация создает нашу новогоднюю атмосферу. Замысловатые узоры возникают из-за огромнейшей разницы между температурами на улице и в помещении.
Да, оказывается именно десублимация создает нашу новогоднюю атмосферу. Замысловатые узоры возникают из-за огромнейшей разницы между температурами на улице и в помещении.